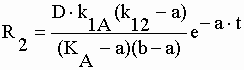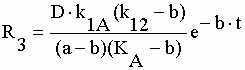Chapitre II Etude des systèmes et modélisation |
|||||||||||||||||||||||||||||||||||||||||||
| III. Administration du marqueur par voie extravasculaire. | |||||||||||||||||||||||||||||||||||||||||||
| Lorsque le marqueur en
analyse de flux métaboliques ou le médicament en pharmacocinétique est administré par
une voie autre que la voie sanguine telle que les voies orale, intrapéritonéale,
sous-cutanée, sublinguale, etc. …, il apparaît dans le sang avec un délai plus ou
moins long. La concentration plasmatique du marqueur ou du médicament augmente
progressivement, atteint une valeur maximale puis diminue jusqu'à disparaître (Intro.
Fig. 3). La forme de la courbe des concentrations est caractéristique d'un
pro-compartiment central que nous désignerons comme le "compartiment
d'absorption". En pharmacocinétique, de nombreux médicaments sont administrés par
voie orale ou "per os", l'ensemble tube digestif et foie (Introd. Fig. 1)
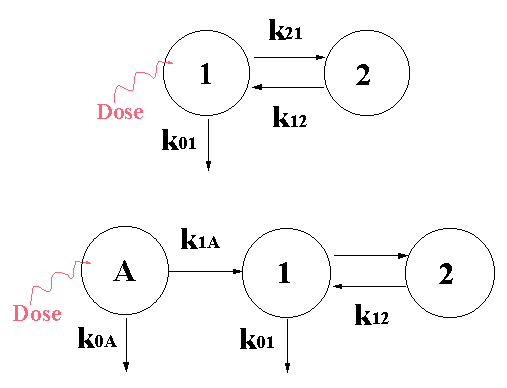
représente le compartiment d'absorption privilégié. En analyse de flux métaboliques, les voies extravasculaires sont moins utilisées que la voie intraveineuse. Dans la mesure où l'on cherche à atteindre la substance endogène ou "marqué" dans son environnement physiologique constitué des liquides plasmatique, interstitiel et cellulaire, c'est la voie IV qui renseigne le mieux sur les systèmes étudiés. L'absorption de l'eau par le tube digestif est très rapide et l'administration du marqueur per os est presque équivalente à l'injection IV. Le métabolisme de l'eau ne nous paraît pas idéal pour bien observer les différences cinétiques associées au mode d'administration du marqueur. Nous choisirons donc le système pharmacologique simple et bien connu de la théophylline. Les modèles théoriques pour cette substance après injection par IV et VO sont comparables à ceux du système eau à 2 compartiments (Fig. II-5, éq. II-39 à 56) nonobstant les différences de nature des molécules étudiées, endogène pour l'eau et exogène pour la théophylline, d'intensité des échanges, de volume des compartiments. Les modèles théoriques suivant les modes d'administration de la théophylline sont représentés ci-dessous (Fig. II-7). La constante d'absorption "k1A" est la résultante des mouvements bidirectionnels entre les compartiments A et central. |
|||||||||||||||||||||||||||||||||||||||||||
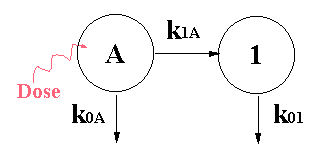
Figure II-7 : Modèles du métabolisme de la théophylline chez un individu jeune. La flèche rouge ondulée représente l’injection d’une dose de médicament par IV (modèle du haut) ou par VO (modèle du bas). Le compartiment A ou d'absorption représente l'ensemble tube digestif et foie. |
|
||||||||||||||||||||||||||||||||||||||||||
| Avec ou sans compartiment d'absorption la technique d'élaboration du modèle mathématique du système théophylline est la même. Les formules II-39 à 56 pour le système eau à 2 compartiments sont utilisables pour le système théophylline. Il ne reste plus qu'à construire le modèle mathématique pour le système avec compartiment d'absorption et tout d'abord le réseau d'équations différentielles linéaires : | |||||||||||||||||||||||||||||||||||||||||||
| dqA/dt
= – KA qA dq'1/dt = + k1A qA – K1 q'1 + k12 q'2 dq'2/dt = + k21 q'1 – k12 q'2 |
II-96 | ||||||||||||||||||||||||||||||||||||||||||
| puis leurs transformées de Laplace : | |||||||||||||||||||||||||||||||||||||||||||
| s FA
– D = – KA FA s F1 = + k1A FA – K1 F1 + k12 F2 s F2 = + k21 F1 – k12 F2 |
II-97 | ||||||||||||||||||||||||||||||||||||||||||
| et l'équation matricielle : | |||||||||||||||||||||||||||||||||||||||||||
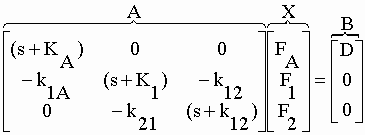 |
|
II-98 | |||||||||||||||||||||||||||||||||||||||||
| La matrice carrée [A] (éq. II-98) diffère de celle de l'équation II-41 par l'addition de la ligne 1 et de la colonne 1 correspondant à l'apport du compartiment d'absorption. Le déterminant est alors : | |||||||||||||||||||||||||||||||||||||||||||
| |A| = (s+KA)
[s2 + s (K1+k12) + (K1K2
-k12k21)] = (s + KA) (s + a) (s + b) . |
II-99 | ||||||||||||||||||||||||||||||||||||||||||
| Les constantes "a et b" de l'équation II-99 étant rigoureusement identiques à celles de l'équation II-42, les expressions intermédiaires "x et y" des équations II-43 sont utilisées telles quelles dans les équations II-100 ci-dessous : | |||||||||||||||||||||||||||||||||||||||||||
| x = a + b = K1
+ k12 y = ab = K1k12– k12k21 = k01k12 |
II-100 | ||||||||||||||||||||||||||||||||||||||||||
| Seules les expressions mathématiques ayant trait au compartiment central seront développées. L'expression de la transformée F1 est obtenue par la règle de Cramer. Au numérateur, la deuxième colonne de la matrice [A] (éq. II-98) est remplacée par le vecteur [B] : | |||||||||||||||||||||||||||||||||||||||||||
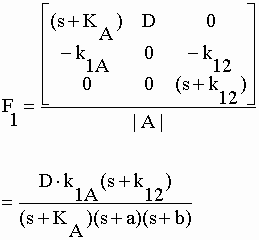 |
II-101 | ||||||||||||||||||||||||||||||||||||||||||
| L'équation II-101 présente 3 pôles "s = - KA, s = - a et s = - b". La fonction "q'1" est donc la somme de 3 résidus : | |||||||||||||||||||||||||||||||||||||||||||
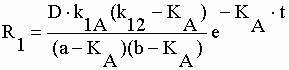
|
II-102 | ||||||||||||||||||||||||||||||||||||||||||
| Posons l'équation à 3 exponentielles de la courbe des concentrations plasmatiques en théophylline qui est la somme des résidus (éq. II-102) divisés par le volume "V1" du compartiment central (éq. II-47) : | |||||||||||||||||||||||||||||||||||||||||||
| c'1 = X exp(- KA t ) + A'1 exp(- a t ) + B'1 exp( - b t ) | II-103 | ||||||||||||||||||||||||||||||||||||||||||
| On peut vérifier que
pour t = 0 la somme des coefficients exponentiels "X + A1 + B1"
est nulle, ce qui est logique puisque au moment de l'injection la théophylline est
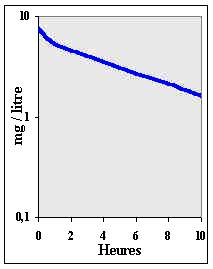
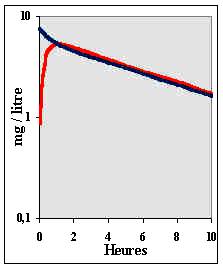
entièrement dans le compartiment d'absorption et absente du compartiment central. La figure II-8 montre les courbes de concentrations plasmatiques en théophylline en fonction des heures suivant l'injection d'une dose de 150 mg du médicament soit par IV soit par VO à un seul individu jeune de 60 kg (modifié d'après Leblanc et Aiache, in "Traité de Biopharmacie et Pharmacocinétique", Aiache et al. Eds, Vigot, Paris, 1985, 105 et d'après Robinson, in "Topics in Clinical Pharmacology and Therapeutics", Maronde Ed, Springer-Verlag, 1986, 1). |
|||||||||||||||||||||||||||||||||||||||||||
Figure II-8 : Concentrations plasmatiques en théophylline après injection d’une dose de médicament par IV (courbes bleues à gauche et à droite) ou par VO (courbe rouge à droite). Coordonnées semi-logarithmiques. |
|
||||||||||||||||||||||||||||||||||||||||||
| L'équation de la courbe bleue après injection par IV est : | |||||||||||||||||||||||||||||||||||||||||||
| c1 = 1,56 exp(-2,2 t) + 5,94 exp(-0,13 t) | II-104 | ||||||||||||||||||||||||||||||||||||||||||
| que nous exprimerons algébriquement par : c1 = A1 exp(- a t) + B1 exp(- b t) et celle de la courbe rouge après administration per os par : | |||||||||||||||||||||||||||||||||||||||||||
| c'1 = -19,2658 exp(-2,5 t) +13 exp(-2,2 t) + 6,2658 exp(-0,13 t) | |||||||||||||||||||||||||||||||||||||||||||
| exprimée algébriquement par : | |||||||||||||||||||||||||||||||||||||||||||
| c'1 = X exp(- KA t) + A'1 exp(- a t) + B'1 exp(- b t). | |||||||||||||||||||||||||||||||||||||||||||
| A partir de l'équation II-103 on extrait tous les paramètres possibles à l'instar de ce qui a été fait pour le métabolisme de l'eau (éq. II-52 à 56 et II-63 à 76). Comme la théophylline est une substance exogène destinée à disparaître (système en état non stationnaire) seules les clairances et non les flux ont été calculées. Le tableau II-4 résume les résultats obtenus. | |||||||||||||||||||||||||||||||||||||||||||
Tableau II-4 : Paramètres du système théophylline calculés à partir de l'injection par intraveineuse du médicament. |
|
||||||||||||||||||||||||||||||||||||||||||
| A présent calculons les
paramètres qu'il est possible d'appréhender à partir de l'équation II-104 des
concentrations de théophylline administrée par VO. Les clairances et volumes
déterminés après injection par IV (tableau II-4) sont des caractéristiques du système
et conservent leur validité quel que soit le mode d'administration du médicament. On démontre que la dérivée au temps t = 0, exprimant la pente à l'origine de l'équation décrivant l'évolution de la quantité totale q'1 de théophylline dans le compartiment central, est égale à la constante d'absorption "k1A". La dérivée à l'origine de la courbe rouge (Fig. II-8 ; éq. II-104) des concentrations "c'1" est donc égale à "k1A D / V1" où le rapport " D / V1" sert de facteur de proportionnalité entre la quantité "q'1" et la concentration "c'1". En effet, au temps t : |
|||||||||||||||||||||||||||||||||||||||||||
| dc'1 / dt = –[KA X exp(- KA t) + a A'1 exp(- a t) + b B'1 exp(- bt)] | |||||||||||||||||||||||||||||||||||||||||||
| et au temps t = 0 : | |||||||||||||||||||||||||||||||||||||||||||
| dc'1 / dt = – [KA X + a A'1 + b B'1] | II-105 | ||||||||||||||||||||||||||||||||||||||||||
| En remplaçant dans l'équation II-105 chaque coefficient exponentiel par son expression tirée des résidus "R1...3" (éq. II-102) on obtient la constante d'absorption : | |||||||||||||||||||||||||||||||||||||||||||
| k1A = – (KA X + a A'1 + b B'1) V1 / D | II-106 | ||||||||||||||||||||||||||||||||||||||||||
| Numériquement, pour D = 150 mg de théophylline et V1 = 20 litres (Tab. II-4), k1A = 2,5/h est identique à la constante d'exit total "KA" de la théophylline hors du compartiment d'absorption. Ce qui signifie que le médicament est absorbé à 100 % (coefficient F de biodisponibilité égal à 1). D'après la littérature, le coefficient de biodisponibilité de la théophylline est voisin de 0,95. Il est clair qu'une variation du coefficient de biodisponibilité F, indépendamment de toute variation des autres paramètres, influe sur la courbe des concentrations plasmatiques en médicament. (Fig. II-9) : | |||||||||||||||||||||||||||||||||||||||||||
| La surface sous la courbe est calculée à partir de l'équation des concentrations plasmatiques (éq. II-104) : | |||||||||||||||||||||||||||||||||||||||||||
| AUCVO = X1 / KA + A'1 / a + B'1 / b | II-107 | ||||||||||||||||||||||||||||||||||||||||||
| Elle est ici égale à AUCIV (Tab. II- 4), ce qui implique que le coefficient de biodisponibilité est aussi mesurable directement par le simple rapport des surfaces sous les courbes "AUCVO / AUCIV". | |||||||||||||||||||||||||||||||||||||||||||
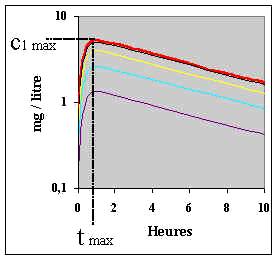
Figure II-9 : Effet de variations hypothétiques du coefficient de biodisponibilité F sur la courbe des concentrations plasmatiques en théophylline après son administration par VO. De haut en bas F = 100, 95, 75, 50 et 25 %. Représentation en coordonnées semi-log. |
|
||||||||||||||||||||||||||||||||||||||||||
| Parmi les informations intéressantes de la courbe après VO, le couple "concentration maximale c'1max et temps correspondant "tmax" (Fig. II-9) permet de visualiser l'intensité d'absorption d'un médicament administré par VO. En effet, elle augmente lorsque "c'1max" augmente et lorsque "tmax" diminue et, inversement, elle diminue lorsque "c'1max" diminue et lorsque "tmax" augmente. Ainsi l'intensité d'absorption de la théophylline varie dans le même sens que "c'1max" (Fig. II-9). On peut estimer graphiquement les valeurs de "c'1max" et "tmax" en visualisant les coordonnées du point au sommet de chacune des courbes expérimentales. On part du fait que la tangente à la courbe en ce point est horizontale et de pente nulle, c'est-à-dire que : | |||||||||||||||||||||||||||||||||||||||||||
|
dc'/dt II-108 = – KAX exp(– KAtmax ) – aA'1exp(– atmax ) – bB'1 exp(– btmax) = 0 |
|||||||||||||||||||||||||||||||||||||||||||
| On obtient tmax
= 1,026 h et c'1max = 5,362 mg / l lorsque F = 100 % (Fig II-9). Ce résultat
est accessible par itération (méthode de calcul répétitif, par exemple
"solveur" du tableur Excel 97 de Microsoft, qui permet la convergence au plus
près de la solution recherchée). Si le système est monocompartimental (Fig. II-10) la résolution de c'1max et de tmax est facilitée car l'équation de c'1 est réduite à 2 exponentielles : |
|||||||||||||||||||||||||||||||||||||||||||
| c'1 = X exp(– KA t) +A'1 exp(– k01 t) | II-109 | ||||||||||||||||||||||||||||||||||||||||||
| avec | |||||||||||||||||||||||||||||||||||||||||||
| X = D k1A / [V1 (k01 – KA)] et A'1 = D k1A / [V1 (KA – k01)] | |||||||||||||||||||||||||||||||||||||||||||
| que l'on écrit plus simplement : | |||||||||||||||||||||||||||||||||||||||||||
| c'1 = [exp(– KA t) – exp(– k01 t)] D k1A / [V1 (k01 – KA)] | |||||||||||||||||||||||||||||||||||||||||||
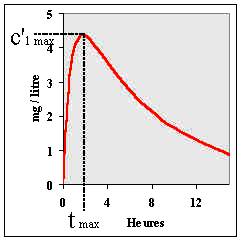
Figure II-10 : Système mono-compartimental avec compartiment d'absorption A.
Courbe des concentrations plasmatiques en substance injectée. |
|
||||||||||||||||||||||||||||||||||||||||||
| De l'équation II-109 on tire la dérivée à t = tmax : | |||||||||||||||||||||||||||||||||||||||||||
| dc'1
/ dt II-110 = D k1A / (k01 – KA) [k01 exp(– k01 tmax) – KA exp(– KA tmax)] = 0
|
|||||||||||||||||||||||||||||||||||||||||||
| d'où les égalités successives : | |||||||||||||||||||||||||||||||||||||||||||
| k01 D
k1A exp(– k01 tmax) / (k01 – KA)
= KA D k1A exp(– KA tmax) / (k01 – KA) |
II-111 | ||||||||||||||||||||||||||||||||||||||||||
| k01
exp(– k01 tmax) = KA exp(– KA tmax)
tmax = – ln (k01 / KA) / (KA – k01) c'1max = D k1A / (k01 – KA) [exp(– KA tmax) – exp(– k01 tmax)] |
|||||||||||||||||||||||||||||||||||||||||||
| La courbe de la figure II-10 concernant une substance quelconque a pour équation : | |||||||||||||||||||||||||||||||||||||||||||
| c'1 = 6,082 [exp(– 0,13 t) – exp(– 1,5 t)] | II-112 | ||||||||||||||||||||||||||||||||||||||||||
| où le coefficient exponentiel A'1 = -X1 = 6,082 mg / litre, les constantes exponentielles sont KA = 1,5 / h et k01 = 0,13 / h. La dose D de substance injectée est de 250 mg. Le volume apparent du compartiment central V1 = 12 litres a été estimé après injection par IV de la même dose. De ces données on tire la constante d'absorption : | |||||||||||||||||||||||||||||||||||||||||||
| k1A = V1 X1 (k01 – KA) / D = V1 A'1 (KA – k01) / D = 0,400 / h | |||||||||||||||||||||||||||||||||||||||||||
| le coefficient de biodisponibilité de la susbstance : | |||||||||||||||||||||||||||||||||||||||||||
| F = k1A / KA = 0,267 ou 26,7 % | |||||||||||||||||||||||||||||||||||||||||||
| les coordonnées de la concentration plasmatique maximale : | |||||||||||||||||||||||||||||||||||||||||||
| tmax =
ln (KA / k01) / (KA – k01) = 1,785 h c'1max = A'1[exp(– k01 t) – exp(– KA t)] = 4,404 mg / litre. |
|||||||||||||||||||||||||||||||||||||||||||